现阶段腐蚀实验是探究金属腐蚀以及防护的主要手段,通过腐蚀实验可以探究金属发生腐蚀的规律及机理、检查并筛选金属材料的材质、估算金属材料的使用寿命、分析金属材料腐蚀事故的原因以及验证防腐蚀的效果等。目前探究金属腐蚀以及防护的方式有多种,如表面分析法、失重法以及电化学法。因为大部分金属产生的腐蚀都是电化学腐蚀,而腐蚀过程中发生的电化学反应为电化学腐蚀的本质,所以金属/电解质界面(双电层)的电化学性质被大量使用于探究金属腐蚀发生的规律、腐蚀产生的机理等方面。因此,在现有的研究金属腐蚀与防护的方法中,电化学方法是一种较为重要的方法。腐蚀电化学法能够按照腐蚀金属电极特点的不同而分为以下三种类型:①. 电化学动力研究方法,指利用控制极化电流及电极电位来测定腐蚀体系中的热力学参数;②. 独用的腐蚀电化学测量跟研究法,指按照金属电化学腐蚀的独特性建立相应的电化学测量跟研究方法;③. 通过模拟装置来探究具有独特腐蚀形态的电化学测试技术,如模拟SSRT裂纹尖端的装置、研究缝隙腐蚀的闭塞电池等。这几种方法中最基础的为电化学动力法。
电极电位以及电流密度为腐蚀电化学实验所要获得的重要参数,其中电极电位表示电解液-金属界面的特性和结构;电流密度表示金属材料表面上单位面积内电化学反应进行的快慢。绝大多数电化学测试都是测定电极电位跟电流密度这两者间的关联。
与其他电化学过程(如电镀、电解及化学电源等)相比,金属电化学腐蚀测量过程的对象是金属电极,该过程有如下特点:
1. 金属发生腐蚀的整个腐蚀体系由数个电极反应耦合而成,同时在整个电极表面上也发生着数个电极反应,所以与只具有一个电极反应的电极系统相比,其在分析和处理腐蚀电化学实验结果上有着一定特别之处。
2. 电极金属材料发生阳极溶解反应,即腐蚀金属自身参与的反应是电极系统中电极反应中的一种。
3. 测量过程中不可以只探究整个电极表面总的电化学行为,因为电极表面表现为多层结构,金属电极上有着腐蚀产物锈层、腐蚀孔及表面膜,导致电极表面具有不光滑的特点,容易发生各种形式的局部腐蚀,所以有必要发展如微区电化学测试之类的能够表征电极表面不均匀性的研究方法。
4. 腐蚀金属的电极反应相对于其他一些电化学过程而言比较缓慢。
此外,腐蚀电化学测试方法为原位技术,能够比较真实地反应金属电极表面发生的实际腐蚀,拥有较强的灵敏度、操作简单容易实施且实时性好的优点。电化学实验常用的方法有极化曲线、交流阻抗及电位扫描等。
极化曲线的测量有利于研究电极过程的影响因素和机理。众所周知,当我们探究可逆电池的反应时电极上基本上是不存在电流的,各个电极的反应基本都在平衡状态下发生,所以该反应为可逆的。但是一旦存在电流通过,电极原本的平衡状态就被打破,进而导致电极电位偏离原本的平衡电位值,导致电极反应处于一种不可逆的状态,不可逆程度随着电极电流密度的升高而增强,即所谓的电极极化就是指由于电流通过电极而导致电位偏离平衡值的一种现状,极化曲线即表示电极电位与电流密度两者间的关系,其测试有以下几种方法。
a. 恒电位法
恒电位法即将被研究的电极电位固定在不同的电位上,然后测试对应电位下的电极电流密度,在实际应用过程中使用较为普遍的是静态法及动态法。所谓静态法是指控制电极电位为某一个特定值,测量相对应电位下的电流密度,且依次测定整个电极电位下的电流密度,从而得到整个极化曲线;其次动态法指控制电极电位按照较为缓慢的速度不停地变化,并且测量相对应电位下的电流值,瞬时电流与其相对应的电位关系曲线即为极化曲线。这两种方法中较为广泛使用的是动态法测定极化曲线,该方法的优点在于扫描速度可以控制、可以自动测量并绘制极化曲线,其测量的结果有较高的重现性,对于那些需要比较的实验该方法为首选。
b. 恒电流法
恒电流法是指固定电极体系的电流密度为某一特定值,测定跟电流密度相对应的电极电位。恒电流法测量极化曲线在测定过程中电极很难达到一个稳定的状态,所以在实际测量过程中一般当电位接近稳定的时候即可以读值。
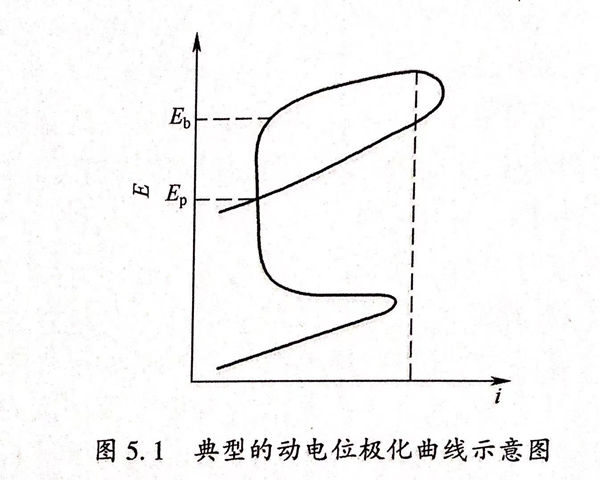
典型的动电位极化曲线如图5.1所示。图中Eb为金属材料的点蚀电位,Ep为保护电位。同样的实验状态下点蚀电位(Eb)值越大则意味着金属产生点腐蚀的倾向越低;当几种金属材料的点蚀电位值相当,只有将点蚀电位和保护电位综合考虑才能评价金属的耐蚀能力,(Eb-Ep)差值越低表明材料钝化膜修复能力越强,耐孔蚀性能越优,因而保护电位(Ep)和点蚀电位(Eb)是被用来表示金属耐孔腐蚀能力大小的基本参数。在E>Eb的条件下,点蚀必然会发生,不但原来具有的蚀孔会长大而且还会产生新的蚀孔;在E<Ep的情况下不会发生点蚀,原来的孔蚀不会长大而且新的蚀孔也不会产生;在Ep<E<Eb条件下,孔蚀存在,原有的蚀孔会接着扩展并生长,但是新蚀孔不会产生。
电化学阻抗谱(Electrochemical Impedance Spectroscopy,EIS),在早期的电化学文献中电化学阻抗又被称为交流阻抗(Alternating Current impedance,AC im-pedance).电化学阻抗原先被用于电学中来探究线性电路网络频率响应特征,后来被用在电极上,进而成为电化学的研究方式。电化学阻抗谱的原理是指向电化学体系施予一频率各异的小振幅交流电动势,测定正弦波频率(ω)的改变对该电动势与电流信号比值产生的影响,即测定阻抗随着正弦波频率(ω)的变化,也可以通过测定阻抗的相位角Φ随ω的变化来分析电极材料、腐蚀机理、导电材料、电极过程的动力学等方面的机理。采用小振幅的电信号既能够防止给系统带来较大的影响,同时又能够让扰动跟响应体系之间表现为近似线性的关系,进而让测量的结果数学处理更容易。此外,电化学阻抗谱是通过测量过程中获得的频率比较宽的阻抗谱探究电极的,所以相对于另外一些电化学法其能够得到电极界面结构和动力学信息。例如:通过阻抗谱形状能够探究金属电极发生腐蚀的机理;探究金属表面上保护膜的阻抗特征;对腐蚀金属进行电化学阻抗测量可以获得极化电阻(Rp);对腐蚀的金属材料进行电化学阻抗谱测量,能够了解动力学参数进而来研究金属材料抗腐蚀能力的强弱等。因此,电化学阻抗谱成为近年来探究金属发生腐蚀与采取相应防护措施的重要方式。
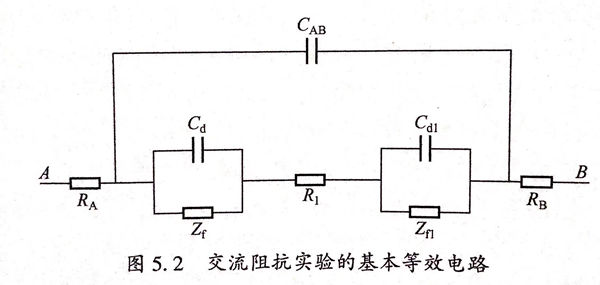
电化学阻抗(EIS)测试把电化学系统作为一个等效电路,交流阻抗实验的基本等效电路如图5.2所示。该电路的组成元件有电阻(R:金属材料对电流的阻拦功能)、电感(L:于电路中对交流电的阻碍功能)及电容(C:电路中对交流电所引起的阻碍作用)等,这些元件按照串联或者并联的方式组合起来形成一个等效电路。测量电化学阻抗能够确定等效电路的组成方式及各组成元件的值、通过这些元件的电化学含义就可以分析电化学电极过程的性质和电化学系统的结构。