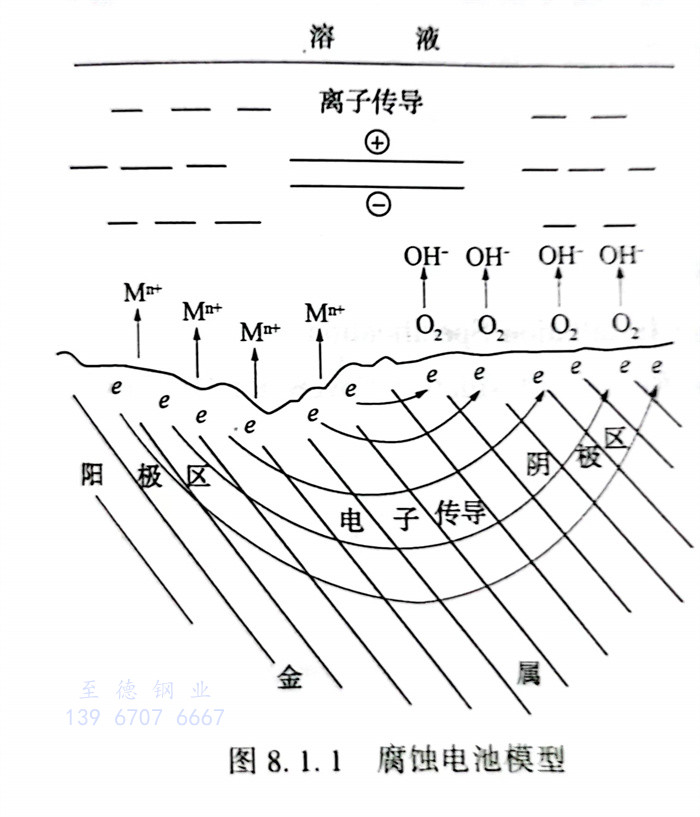
电化学腐蚀是指金属表面与离子导电的介质发生电化学反应而引起的破坏,是至少包含一对电极反应的腐蚀。电化学腐蚀是最普遍、最常见的腐蚀,例如金属在大气、海水、土壤和各种电解质溶液中的腐蚀都属此类。
阳极和阴极是电接通的,电子可以在其间流动,它们接触的电解液也是连通的,离子可以在其间流动。图8.1.1是一个腐蚀电池的模型。金属表面存在电位不同的阳极和阴极,是由于表面含有杂质,不完整的氧化膜,不同的结构,以及和表面接触的溶液不均一,如浓度、成分、含氧量、温度等不同,根据能斯特公式表面各部分电位也将不同,电位较低部分是阳极,阳极反应是金属的离子化(即腐蚀),金属离子进入溶液,同时有相应的电子留在表面。如果阳极是孤立的,随着表面电子的增多,会迅速达到平衡,金属腐蚀将实际停止。由于表面存在电位较高(正)的阴极,电子就可能从阳极源源不断流到阴极,在那里产生吸收电子的反应,阳极腐蚀因而不断进行。