从图5.22中可以看出,不同表面粗糙度的试样的极化曲线都具有活性溶解-钝化转变的特征,并且都具有三个自腐蚀电位。当电位低于Ecorr-1时,三条曲线的腐蚀电流密度相差很小。因此为了简化讨论可以认为具有不同表面粗糙的试样的阴极反应(H+的还原反应)是相同的,不随表面粗糙度的变化而变化。金属的阳极溶解电流随着表面粗糙度的增加而增加,这种现象可以用金属的表面功函数(EWF)来解释。EWF是指材料的自由电子脱离材料表面的最低能量。金属的暴露面积越大材料失去电子被氧化的概率就越高,且EWF随着材料的表面粗糙度的增加而降低,表面粗糙度大的试样具有较低的EWF和较大的有效暴露面积,因此越容易失去电子,从而加速材料的腐蚀过程。
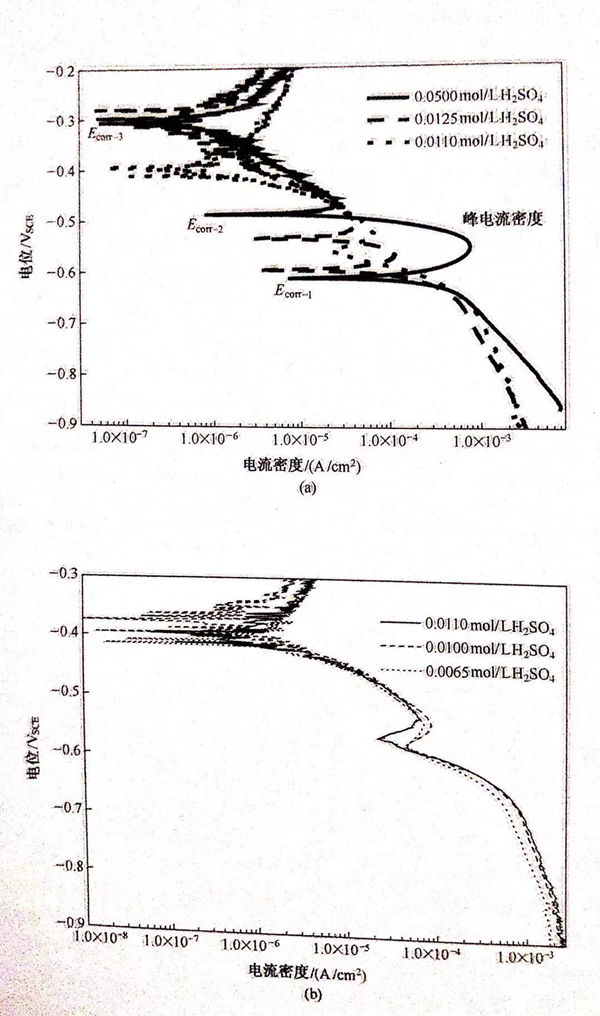

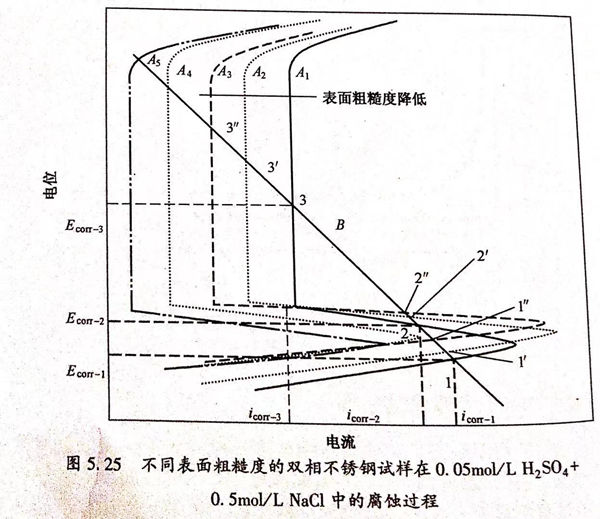
图5.25的理论极化曲线可以用来解释不同表面粗糙度的双相不锈钢的腐蚀过程。图5.25中A1、A2、A3分别代表理论阳极极化曲线,B代表理论阴极极化曲线,阴、阳极极化曲线的交点个数即代表了自腐蚀电位的个数。假设B和A1分别代表240号砂纸打磨后的试样的理论阴、阳极极化曲线,因此测量的极化曲线就是二者的代数叠加,从图5.25中可以看出A1和B有三个交点(1、2、3),即表示有三个自腐蚀电位。当表面粗糙度降低(800号和抛光试样)时,阳极极化曲线变为A2和A3,从图5.25中可以看到仍然出现了三个交点(1'、2'、3')和(1”、2"、3”),即有三个自腐蚀电位。不同表面粗糙度的试样的自腐蚀电位有如下关系:Ecorr-1<Ecorr1'<E corr-1",E corr-2<E corr-2,<E corr-2",E corr-3<Ecor-3/<Ecorr-3”。如果阳极极化曲线转变为A4和A5,自腐蚀电位转变为两个或者一个,但是这种情况在本实验条件下没有出现。
从图5.22中可以看出,溶液的pH值可以显著改变双相不锈钢在酸性NaCl溶液中的腐蚀行为,从而使自腐蚀电位的个数随着H*浓度的降低而减少。在酸性NaCI溶液中,主要的阴极反应是H*的还原反应。可以用图5.26中的理论极化曲线来解释pH值改变对自腐蚀电位个数的影响。图5.26中曲线A1、A2和A3分别代表双相不锈钢在不同pH值的溶液中的理论阳极极化曲线,B1、B2和B3代表阴极H+还原反应的理论极化曲线。如果腐蚀过程是由阴极曲线B1和阳极曲线A1耦合而成,那么在金属的活性溶解区、溶解-钝化过渡区和完全钝化区内阴、阳极极化曲线就会有三个交点(1、2、3),也就会出现三个自腐蚀电位。这对应于图5.22(a)中H2SO4浓度大于0.011mol/L的条件下的情况。降低溶液的pH值,就会影响阴、阳极反应的过程,从而改变极化曲线的位置。当阴、阳极极化曲线由B2和A2耦合而成,则只有两个交点,也就是只有两个自腐蚀电位存在。这对应于图5.22(b)中H2SO4浓度介于0.0065~0.011mol/L时的条件下所得到的结果。进一步降低溶液的pH值,使硫酸浓度降为0.005mol/L以下,阴、阳极极化曲线由B3和A3耦合而成,则只有一个自腐蚀电位存在。若进一步降低溶液的pH值,自腐蚀电位的个数将不再发生改变,保持一个。
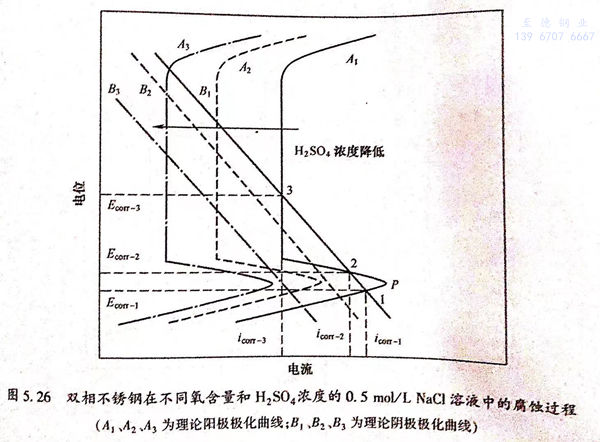
图5.26 双相不锈钢在不同氧含量和H2SO4浓度的0.5mol/L NaCl溶液中的腐蚀过程(A1、A2、A3为理论阳极极化曲线;B1、B2、B3为理论阴极极化曲线)在有氧存在的条件下,溶液中的阴极反应除了H+的还原反应之外,还有氧的还原反应:
O2+4H++4e- = 2H2O
因此,在有氧存在条件下的阴极反应的电流密度是氢还原反应和氧还原反应的电流密度之和。从图5.24中可以看出,溶液中的氧不但能影响阴极反应过程,还能影响阳极反应过程,造成自腐蚀电位正移,腐蚀电流密度增加。可能是由于溶液中的氧含量增加,获得自由电子的概率增加;或者提高氧在金属表面或者钝化膜表面的还原速度。
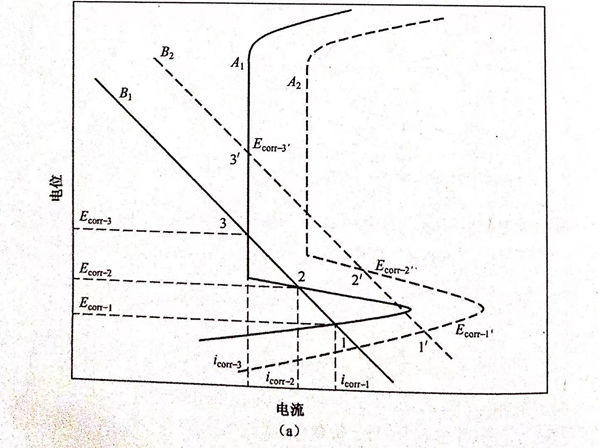
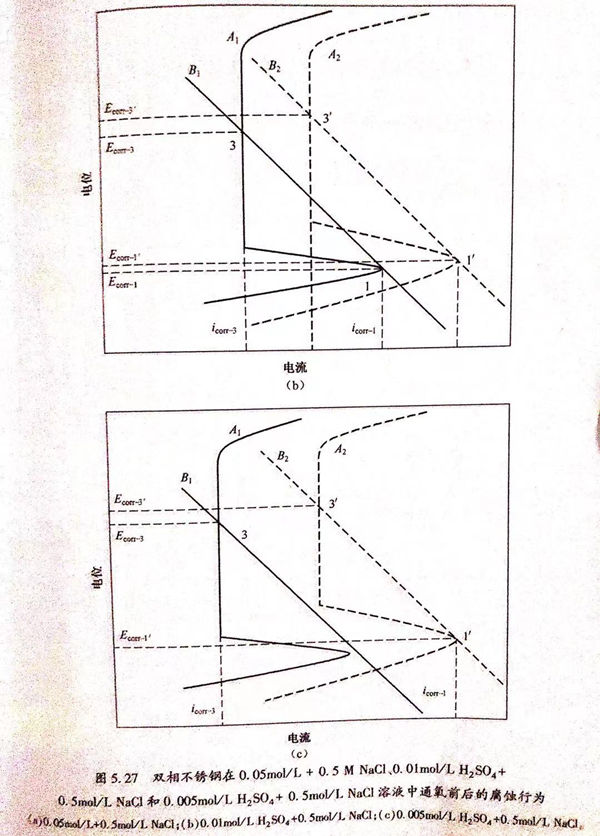
溶液中的氧含量对双相不锈钢在酸性NaCl溶液中的腐蚀行为的影响可以用图5.27来解释。氧对双相不锈钢腐蚀行为的影响与pH的影响效果基本一致。图5.27(a)可用来解释图5.23(a)的实验现象。当溶液中不含氧(氮气饱和)时,B1和A1分别代表理论的阴、阳极极化曲线。从图5.27中可以看出曲线有三个交点,即存在三个自腐蚀电位 ECOrr-1、Ecorr-2和Ecorr-3相对应的腐蚀电流密度为icorr-1、icorr-2和icorr-3.当有氧存在(空气饱和或氧饱和)时,阴、阳极极化曲线分别变为B2和A2,仍然有三个自腐蚀电位Ecorr-1'、Ecorr-2'和Ecorr-3',并且 Ecorr-1'>E corr-1、Ecorr-21>Ecorr-2、Ecorr-3'>Ecorr-3。图5.23(b)中在通氧前后都只有两个自腐蚀电位,这一现象可以用图5.27(b)来解释。当溶液中通入氧前,B1和A1分别代表理论的阴、阳极极化曲线,从图5.27中可以看出曲线有两个交点,即存在两个自腐蚀电位Ecorr-1和Ecorr-3,相对应的腐蚀电流密度为icorr-1和icorr-3。当有氧饱和时,阴、阳极极化曲线分别变为B2和A2,仍然有两个自腐蚀电位 Ecorr-1'和Ecorr-3'。通氧前后自腐蚀电位的关系为Ecorr-1'>Ecorr-1,Ecorr-3'>Ecorr-3.当硫酸浓度为0.005mol/L时,在极化曲线只有一个自腐蚀电位存在,但溶液经过氧饱和后,自腐蚀电位个数由一个增加为两个,这一现象可以用图5.27(c)来解释。空气饱和溶液中的理论阴、阳极极化曲线分别为B1和A1,从图5.27中可以看出只有一个交点,即只存在一个自腐蚀电位;当氧气饱和时,由于氧气促进了阴、阳极反应过程,使阴、阳极极化曲线到达B2和A2,此时曲线有两个交点,即出现两个自腐蚀电位。