缝隙腐蚀具有普遍性,对于金属类型和腐蚀介质没有“选择性”,即几乎全部种类的金属都会发生该类腐蚀,腐蚀性介质都可能造成该类腐蚀。浙江至德钢业有限公司本次主要介绍缝隙腐蚀机理、影响因素、研究缝隙腐蚀的数值方法,并提出相关预防措施。
缝隙腐蚀属于电化学腐蚀的一种类型,其机理包括金属离子浓差电池理论、氧浓差电池理论、活化-钝化电池理论等,其中氧浓差电池理论被大家普遍接受。对于服役于含氯离子环境中的奥氏体不锈钢,氯离子会在缝隙内聚集,引发点蚀,加速缝隙腐蚀,该类腐蚀称为点蚀型缝隙腐蚀。缝隙腐蚀和应力腐蚀相比,前者是局部的全面腐蚀或密度较大的坑蚀。从实际腐蚀案例来看,在氯离子以及拉应力存在的情况下(特别是拉应力较大的情况),生应力腐蚀的概率远大于缝隙腐蚀。
一般认为,在含氧的中性溶液中,缝隙腐蚀是由氧浓差电池引起的。过程如下:
起始阶段,缝隙里面和外面金属的电化学反应一样,都是阳极溶解,主要反应为:
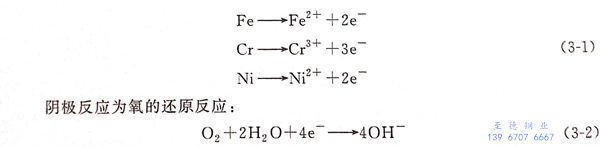
随着反应进行,缝隙内部氧含量降低,又难以补充,造成阴极反应减缓直至停止,但是阳极反应继续进行。为达到反应平衡,缝隙内部的阳极反应只能由外部的阴极反应平衡,造成的结果是:缝隙外面的阴极反应面积大,内部的阳极反应面积小,加速了阳极反应。一方面,缝隙内部由于阳极反应产生的金属离子不易转移到缝隙外面,缝隙外部的阴离子会进入缝隙内部使电荷保持平衡,特别是溶液中含氯离子时,会造成内部氯离子含量升高。另一方面,缝隙内部由于阳极溶解产生的部分金属离子会发生水解,造成氢离子浓度增大,pH值降低。缝隙内部氯离子浓度的升高以及pH值的增加都会加速钝化膜溶解。缝隙腐蚀示意图如图3-1所示。
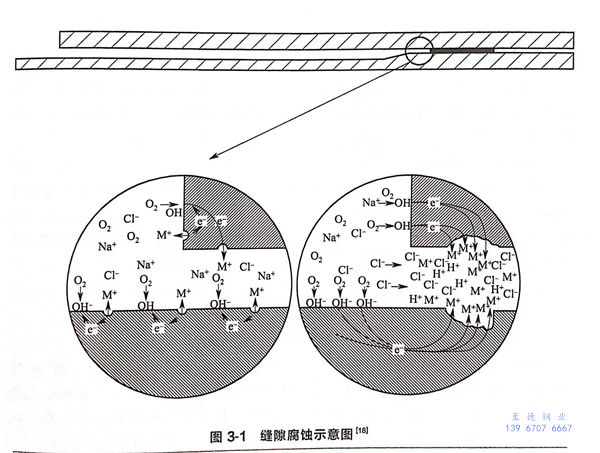
假设材料表面是均匀的,缝隙内外“小阳极”“大阴极”的反应持续进行,则缝隙内会发生全面的缝隙腐蚀。实际上,金属表面的钝化膜会存在缺陷,诸如表面夹杂、化学成分不均匀、晶体缺陷、机械破坏等。在侵蚀性阴离子存在的情况下,这些缺陷部位的钝化膜优先被破坏,发生点蚀或应力腐蚀等更为局部的腐蚀形态。



