要提高不锈钢的耐腐蚀性,首先要注意的是不锈钢的化学成分和组织,这是引起电化学腐蚀的内在原因,而腐蚀介质、温度等是外因;尤其是钢的化学成分,决定着电极电位差的大小和腐蚀电流的大小。
铬是不锈钢都含有的元素,铬是铁素体形成元素。铬的主要作用是耐腐蚀。从图1-3中可以看出在钢中添加铬对腐蚀性的影响。当金属中铬含量达到12%时,在大气环境下或在氧化性介质中铬可以自发形成一种稳定的、透明的、极薄的钝化膜来阻止腐蚀,使金属基本上不会生锈。较高的合金含量可通过强化薄膜和快速自我修复薄膜来提高抗腐蚀性。不锈钢的铬含量上限为30%.在氧化膜中,铬与铁的比例可以有很大的变动,铬最高可达到铁的9倍。这种富铬的氧化膜具有尖晶石点阵,在许多介质中都有很高的稳定性。当钢中铬含量低于10%时,钝化膜中不存在铬的氧化物。
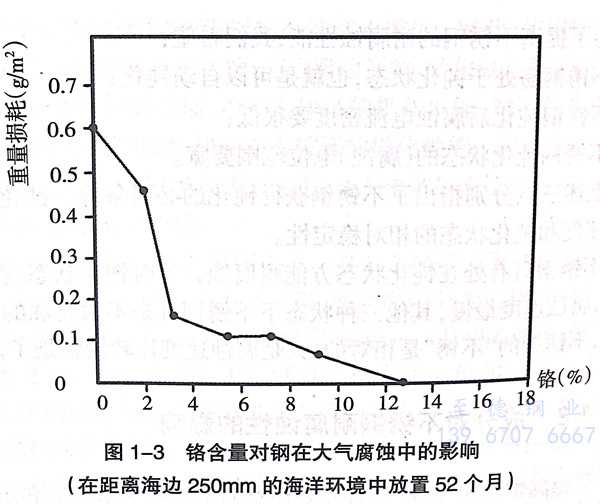
不锈钢所以耐腐蚀,主要是由于其表面有厚10埃以上的富集的铬的氧化物薄膜。这层富集的铬的氧化物薄膜,将其金属与外部环境的联系隔断,达到防腐蚀的目的。这层氧化膜厚度一般在20~30埃之间,成分为Cr2O3,极其致密,与一般化学品不发生反应,氧和腐蚀物质无法通过这层氧化膜腐蚀内部基体。
镍是奥氏体的稳定元素,镍可将奥氏体使用范围扩大到低温区从图1-4可以看出镍的作用。在图1-4中,斜线以上所示温度下奥氏体是稳定的;在这条线以下,铁素体和马氏体都具有稳定的晶体结构。镍可提高韧性和延展性,使之更易于加工、制造和焊接,增强抗酸的腐蚀能力,保持钝化膜的能力及在腐蚀介质中的抗蚀能力。
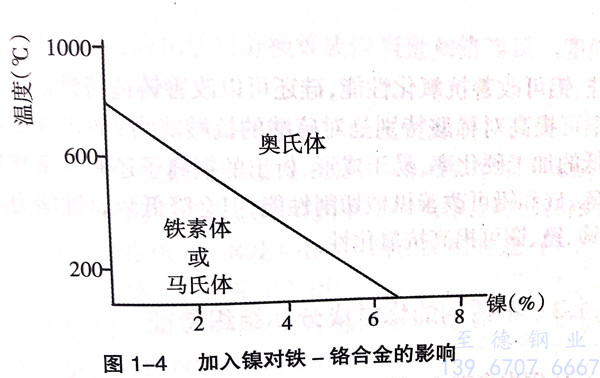
在不锈钢中加入镍时,耐腐蚀性有所改善。镍较难氧化,故氧化膜中镍含量较少;氧化膜下富集了镍,可增加氧化膜的稳定性,尤其是在非氧化性的硫酸中更为显著。将镍加入铬不锈钢中就会提高其在硫酸、醋酸、草酸及中性盐(特别是硫酸盐)中的耐腐蚀性。
锰类似于镍,当添加锰或用锰替代镍时,都会提高不锈钢的强度。在铬不锈钢中加入锰(在Cr≥17%的情况下),对钢的耐蚀性没有多大的影响。但锰可以大大提高铬不锈钢在有机酸(如醋酸、甲酸、乙醇酸)中的耐腐蚀性,促使铬不锈钢达到钝化状态,在这方面锰的作用比镍的用更明显。
钼可提高钝化膜的强度,增强耐局部腐蚀性,如耐点蚀、缝隙腐蚀,特别是在卤盐或海水中有氯离子的情况下。钼也可提高对氯化物应力腐蚀断裂的抵抗能力。利用固溶强化的方法,钼可提高奥氏体不锈钢的高温强度和马氏体不锈钢的抗回火能力。
钼能提高不锈钢的钝化能力,扩大不锈钢的钝化介质范围。如在热硫酸、稀盐酸、磷酸及有机酸中,含钼的不锈钢都有满意的使用效果。不锈钢中加入钼,可以形成含钼的氧化膜。这种含钼的氧化膜具有更高的稳定性,在许多强腐蚀介质中都不易溶解。它还可以防止卤族元素离子(特别是氯离子)对氧化膜的破坏。因为氯离子半径很小,可以穿透不够致密的氧化膜,与钢起作用,生成可溶的腐蚀产物,在局部区域形成点腐蚀。含钼的氧化膜对氯离子有足够的稳定性。
氮是稳定奥氏体的元素,可提高钢的强度,在奥氏体及双相不锈钢中可增强耐点蚀及缝隙腐蚀的能力,并减少金属间相(σ)在高温或焊接时析出的机会。
金属间相是指由钢中的两种或两种以上的金属元素构成的金属间化合物,也简称为中间相。广义地讲,凡以元素周期表中过渡族元素(锰、铁、钴和镍等)为基体,含有A副族元素(钛、钒和铬等)的合金系在适合生成的条件下都能形成一系列金属间相。
钛、铌能优先与碳和氮结合形成碳化物和氮化物,改善高温强度性能并阻止铬的碳化物的形成,防止晶间腐蚀。铌还可提高高温蠕变断裂强度。
硅、铝可改善抗氧化性能,硅还可以改善铸造特性。
铜可提高对稀酸特别是对硫酸的抗酸能力;加入3%~4%的铜具有低的加工硬化率,易于成形,析出的铜离子还有灭菌作用。
硫、硅和铅可改善机械切削性能,但会降低耐腐蚀能力。
铈、镱、镧可提高抗氧化性。



