有关环境因素对耐腐蚀性影响的研究,主要是以304不锈钢或316不锈钢为对象来研究离子的种类、温度的影响。日野(1958~1961年)研究了氯化物的种类、温度、pH值、还有流动速度对18Cr-8Ni钢发生点腐蚀的影响。在氯化物中,FeCl3和CuCl2能引起高度腐蚀;而且在40~80℃的温度范围内,温度越高,点腐蚀发生的几率越高;此外在pH值低的情况下会发生全面腐蚀,pH值是4~5时会发生点腐蚀,而pH值为7时点腐蚀的发生会减少。此外,在氯化铁溶液中进行的有关流动速度影响的试验表明,流动速度提高后,点腐蚀数量增多,点腐蚀面积减小,并渐渐转为全面腐蚀。前川等(1965年)把304不锈钢和304L不锈钢置于25℃的1mol/dm3 H2SO4溶液中,然后在溶液中添加KCl,得出的阳极极化曲线表明随着KCl浓度的升高,点腐蚀电位降低。藤井等(1970年)也阐明了耐点腐蚀能力随着氯离子浓度、温度的升高而下降这一点。
此后,关于氯化物水溶液中的温度和氯离子影响这一点,Tru-man针对304不锈钢所得出的数据表明,在高温高浓度情况下发生应力腐蚀断裂,温度浓度下降后发生点腐蚀,若继续下降则出现生锈现象。但藤井(1975年)对处于100℃以上的0.1mol/dm3NaCl溶液中的304、316、321不锈钢进行了测定,根据这一测定结果可知:温度越高,点腐蚀电位越低;在260℃的情况下,受氧化膜的影响,重新返回到高电位,耐点腐蚀性也得到恢复。而且还表明了NO3的添加使点腐蚀电位升高。丹野等(1988年)也测定了25~250℃的0.05~1 mol/dm3 NaCl溶液中的304不锈钢的点腐蚀及缝隙腐蚀电位,从而证明了在25~175℃下这两种电位都低,175℃以上点腐蚀电位升高,250℃时则出现全面腐蚀。
另一方面,除氯离子以外,对卤离子和其他阴离子的研究也在积极地进行。森冈等(1964年)认为在卤离子中,Br对18Cr8Ni钢点腐蚀性的影响最大,其次是Cl-,I-,F-.盐原(197年)分别使用25℃的0.5mol/dm3水溶液对304不锈钢和316不锈钢进行了试验,以研究卤离子对缝隙腐蚀的影响,进而证实了缝隙腐蚀电位依次是Cl-<Br-<I-(→高),这与Cl-,Br-对点腐蚀的影响存在异同点。
关于卤离子之外的各种阴离子对含盐水溶液中点腐蚀的影响,森冈等(1964年)证实了OH-、SO4-、NO3-有抑制点腐蚀的效果。而且也证明了添加少量的NO3-后,虽然会暂时出现点腐蚀,但只要进一步提高电位,点腐蚀就会再度停止。此外,铃木等在1971年使用人工蚀孔研究了阴离子对抑制点腐蚀的影响,结果表明氧化性阴离子有抑制蚀孔内活性溶解的作用,按影响的大小顺序排列依次为:NO3,NO2,MnO4,Cr2O/7,CrO24,ClO4。此外,藤井等(1972年)提出,能有效抑制点腐蚀产生的阴离子依次有NO3≥CrO4>WO24->H2PO2,能有效抑制点腐蚀发展的阴离子依次有NO3≥WO4->CrO4>H2PO2.另外根据盐原(1961年)的研究报告,OH、SO4-、NO3使18Cr-8Ni钢的电位升高(即有抑制作用),而对缝隙腐蚀电位几乎没有影响。中田等(1976年)也考察了SO24-的添加对SUS316L在氯化物溶液中的点腐蚀及缝隙腐蚀的影响,结果证明SO4-具有抑制腐蚀产生的效果,而没有抑制活性成分偏析的作用。另外,中川等(1982年)在报告中称,SO4-的添加能抑制:SUS304、316钢缝隙腐蚀的产生与发展。还有冲等人(1984年)通过试验得出,KClO3或K2Cr2O7的添加使304钢在0.5mol/dm3 NaCl溶液中的点腐蚀得到抑制,而Fe2(SO4)3的添加反而加速缝隙腐蚀。
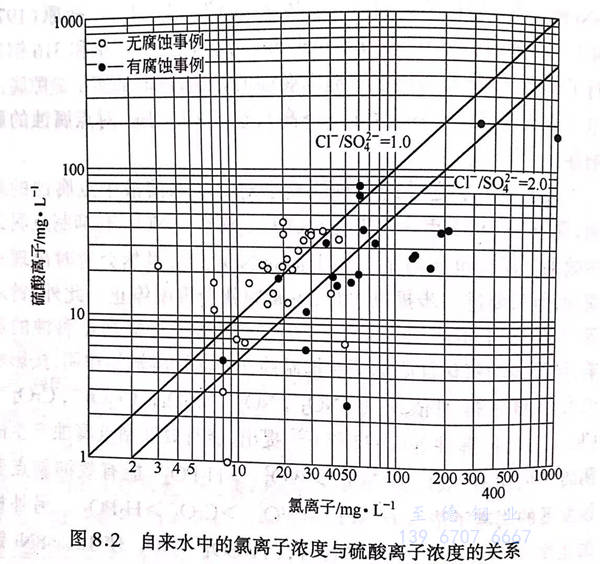
如上所述,多种阴离子都能抑制由氯离子引起的点腐蚀,但使用自来水的室内热水供应管道经常在焊接接口处发生局部腐蚀,通过具体事例对这种局部腐蚀的发生与水质的关系进行了分析,结果得出Cl-和SO4-的影响如图8.2(1998年)所示,这表明自来水中的Cl-与SO4的比值越大,越容易被腐蚀。
另外,关于采用阴极防点腐蚀这一点,北村等(1966年)通过试验证明,利用外部电源法能防止2%NaCl+70%谷氨酸钠溶液中的316L不锈钢出现点腐蚀现象,这种方法同样适用于化学工厂。为了防止在海水中使用的船舶和螺旋桨发生点腐蚀现象,藤井等(1968年)通过海水试验证实了Zn作为动电阳极能防止304不锈钢出现点腐蚀现象。保坂等(1976年)证实了锌元素同样能防止缝隙腐蚀的发生。



