2205双相不锈钢在不同温度的3.5%NaCl溶液以及3.5%NaCl+不同浓度S2-溶液中的极化曲线如图5.44所示。
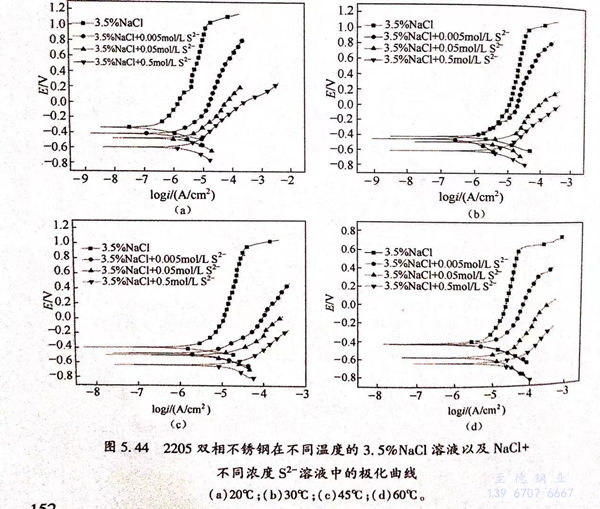
从图5.44中可以看出,双相不锈钢在不同温度的3.5%NaCl溶液中都存在一定范围的钝化区,且钝化区的范围随着溶液温度升高而缩小。当S2-加入至3.5%NaCl溶液中后,双相不锈钢在溶液中的极化曲线与其在3.5%NaCl溶液中的极化曲线相比,整体右移,下移;且加入S2-后,双相不锈钢在溶液中的钝化现象不再明显,钝化区明显缩小,甚至无钝化区。以上说明,S2-使得双相不锈钢在3.5%NaCl溶液中的腐蚀速率加快,降低了双相不锈钢的耐蚀性能。
图5.44中极化曲线的Tafel拟合结果如图5.45和表5.14所示。
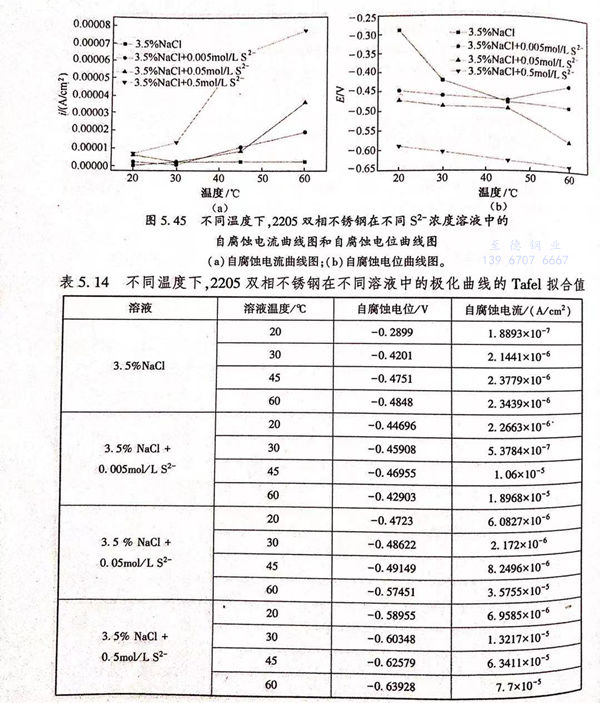
结合图5.45(a)和表5.14可以看出,在相同的溶液中,随着溶液温度的升高,双相不锈钢在3.5%NaCl溶液中的自腐蚀电流密度呈现升高的趋势;在3.5%NaCl溶液中,当溶液温度从20℃升高至60℃时,双相不锈钢在溶液中的自腐蚀电流密度从1.8893×10-7 A/c㎡升高至2.3439×10-6 A/c㎡;在3.5%NaCl+0.005mol/L S2-溶液中,当溶液温度从20℃升高至60℃时,双相不锈钢在溶液中的自腐蚀电流密度从2.2663×10-6升高至1.8968×10-5 A/c㎡;在3.5% NaCl+0.05mol/L S2-溶液中,当溶液温度从20℃升高至60℃时,双相不锈钢在溶液中的自腐蚀电流密度从6.0827×10-6 A/c㎡升高至3.5755×10-5A/c㎡;在3.5% NaCl +0.5mol/L S2-溶液中,当溶液温度从20℃升高至60℃时,双相不锈钢在溶液中的自腐蚀电流密度从6.9585×10-6A/c㎡升高至7.7×10-5A/c㎡.在相同温度下,随着溶液中的S2-浓度的升高,双相不锈钢在溶液中的自腐蚀电流呈现升高的趋势:当溶液温度为20℃时,随着S2-浓度的升高,双相不锈钢在溶液中的自腐蚀电流密度从3.5%NaCl溶液中的1.8893×10-7A/c㎡分别升至2.2663×10-6A/c㎡,6.0827×10-6A/c㎡,6.9585×10-6 A/c㎡;当溶液温度为60℃时,随着S2-浓度的升高,双相不锈钢在溶液中的自腐蚀电流密度从3.5%NaCl 溶液中的2.3439×10-6 A/c㎡分别升至1.8968×10-5A/c㎡,3.5755×10-5A/c㎡,7.7×10-5A/c㎡.从以上分析可知,S2-的加入使得双相不锈钢在3.5%NaCl溶液中的自腐蚀电流密度变大,加速了腐蚀速率。
从图5.45(b)和表5.14中可以看出,在相同的溶液温度下,随着3.5%NaCI溶液中的S2-浓度的升高,双相不锈钢在溶液中的自腐蚀电位呈现下降的趋势。当溶液温度为20℃时,随着溶液中的S2-浓度的升高,双相不锈钢在溶液中自腐蚀电位从-0.2899V分别下降至-0.44696V,-0.4723V,-0.58955V;当溶液温度为30℃时,随着溶液中的S2-浓度的升高,双相不锈钢在溶液中自腐蚀电位从-0.4201V分别下降至-0.45908V,-0.48622V,-0.60348V;当溶液温度为45℃时,随着溶液中的S2-浓度的升高,双相不锈钢在溶液中自腐蚀电位从-0.4751分别变为-0.46955V,-0.49149V,-0.62579V;当溶液温度为60℃时,随着溶液中的S2-浓度的升高,双相不锈钢在溶液中自腐蚀电位从-0.4848V分别变头-0.42903V,-0.57451V,-0.63928V.S2-对双相不锈钢在3.5%NaCl溶液中自腐蚀电位有明显的影响,S2-的加入使得双相不锈钢在3.5%NaCl溶液中的自腐蚀电位下降,增加了双相发生腐蚀的倾向,使腐蚀更易发生。
2057双相不锈钢在1050℃固溶后在室温下于3.5%NaCl,3.5%NaCl+0.005mol/LNa2S、3.5%NaCl+0.05mol/LNa2S及3.5%NaCl+0.5mol/LNa,S溶液中的动电位极化曲线,如图5.46所示。从图5.46中可知在纯的3.5%NaCI溶液中 DSS2507双相不锈钢的自腐蚀电位(Ecorr)较高,自腐蚀电流(Icorr)较低,分别为-0.31637V(vs.SCE),1.1417x10-7(A/c㎡),表明在纯的3.5%NaCl溶液中2507双相不锈钢耐腐蚀性能较好。GB 4334.9-1984规定阳极极化曲线上与电流密度100μA/c㎡相应的电位为击破电位,从图5.46中可知DSS2507双相不锈钢于3.5%NaCl溶液中击破电位(Eb)为1.002V,所以于3.5%NaCl溶液中2507双相不锈钢也有较好的抗点蚀性能。这是由于DSS2507于不含硫离子的3.5%NaCl介质中有明显的钝化区且钝化区域较宽,在该钝化区范围内钢表面会形成一层致密度较高的钝化膜,该膜层有较高的抗蚀性能,进而减弱了DSS2507的腐蚀敏感性。随着硫离子被引入到3.5%NaCl液中,从图5.46可以清晰地看出极化曲线向右下方移动,自腐蚀电位(E)降低,自腐蚀电流(I)升高,DSS2507双相不锈钢的腐蚀速率变快。并且随着硫离子浓度越高阳极极化曲线向右下方移动趋势越明显。从表5.15可知硫离子浓度为0.005mol/L、0.05mol/L及0.5mol/L时的自腐蚀电位(E)与不含硫离子的3.5%NaCl溶液中相比分别降低了0.19703V(vs.SCE),0.22259V(vs.SCE),0.33695V(vs.SCE);Icom分别升高了1.085x10-6A/c㎡、8.97×10-6A/c㎡和6.99×10-5A/c㎡,这表明随硫离子浓度越高,自腐蚀电位(Ecom)降低的越多,但是自腐蚀电流(Icom)涨幅越大,以上现象说明硫离子导致2507双相不锈钢的腐蚀速率加快,抗均匀腐蚀能力降低。
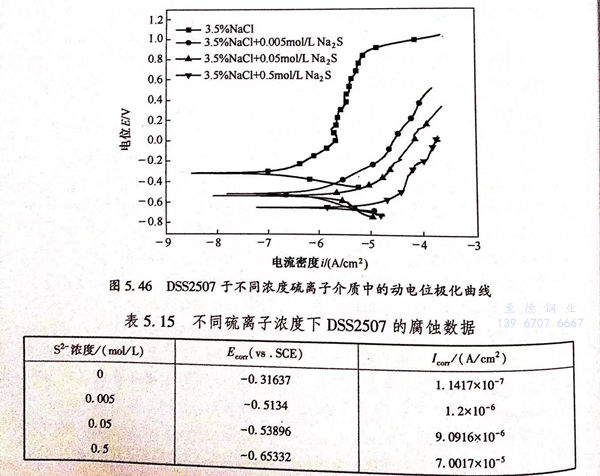
综上所述,硫离子提高了DSS2507双相不锈钢的腐蚀敏感性。双相不锈钢在钝化过程中铬离子通过离子键与O2-或OH-相结合,产生一层致密的成分为Cr的氧化物或Cr的氢氧化物(Cr2O3或Cr(OH)3)的氧化膜,该膜层能够提高材料的抗腐蚀性能,2507双相不锈钢表面钝化膜的保护性对其耐腐蚀性能起着主要作用。但是在硫离子的作用下,由于硫离子的电负性能较强吸附,在金属表面,并且S2-能够代替一部分O2-或OH-的位置,与铬离子相结合阻挡了能够引起钢钝化的物质(OH-、O2-等)接近钢表面,破坏了原来钢表面钝化膜的完整性和致密度,从而降低了金属材料表面钝化膜的生长速度,提高了材料的腐蚀敏感性,减弱了DSS2507双相不锈钢的抗蚀能力。除此之外,硫离子有着破坏钢表面钝化膜结构的作用,使体系的腐蚀电位降低,进而提高了2507双相不锈钢发生均匀腐蚀的倾向,实际表现为腐蚀电位变小,腐蚀电流变大。另一方面阴极反应过程中生成的H+被阳极反应产生的电子还原为氢原子,一部分结合成H2释放出去,另外,吸附在金属表面,通过去吸附溶解到金属内部使这一区域变脆进而引起氢脆。在这两种因素共同作用下硫离子导致2507双相不锈钢的耐蚀能力降低。
图5.47是室温下固溶态为1050℃的DSS2507双相不锈钢分别于3.5%NaCl溶液以及含有0.05mol/L硫离子的3.5%NaCl溶液介质中动电位扫描后的微观组织形貌。图5.47(a)显示当硫离子浓度为0mol/L,即DSS2507双相不锈钢于3.5%NaCl溶液介质中动电位扫描后的微观组织形貌上腐蚀坑数量比较少,零零散散地散布于铁素体(α)上;而当硫离子浓度为0.05mol/L时,从图5.47(b)中可以看出腐蚀点的数量明显增多且分布较密集。这进一步说明硫离子提高了2507双相不锈钢的腐蚀敏感性加速了其腐蚀的发生。



